来源:X-MOL资讯
三烷基胺结构广泛存在于药物、生物碱和农药中,对三烷基胺进行C-H键官能团化是制备其衍生物最高效且原子经济的方法。虽然过渡金属催化胺的C-H键官能团化反应研究在近十几年取得了显著进展,然而,适用于三烷基胺的反应还十分稀少,其原因在于:(1)富电子的三烷基胺在氧化性的反应条件下易分解;(2)三烷基胺较大的位阻难以作为导向基捕获金属催化剂。而且,已报道的反应主要发生在活性较高的氮原子α位,而在烷基链上较远的位置进行C-H键官能团化的难度很大。
近年来,有机硼路易斯酸催化胺的C-H键官能团化反应研究得到了快速发展。有机硼路易斯酸攫取氮原子α位负氢,形成亚胺正离子和硼氢负离子;亚胺正离子去质子化形成烯胺,再与亲电试剂反应,可实现β位C-H键官能团化。然而,该策略存在局限性,其中,β位C-H键官能团化仅适用于活性较高的亲电试剂(如硅正离子、氘质子、缺电子烯烃、靛红或者吲哚-3-酮)。
我校王晓晨课题组一直致力于有机硼路易斯酸催化含氮化合物的官能团化反应研究,近年来利用硼催化剂攫取氮原子α位负氢的这一反应活性,实现了多种胺类化合物的合成以及C-H键官能团化反应(ACS Catal. 2019, 9, 295–300; Angew. Chem. Int. Ed. 2021, 60, 17185–17190; Chin. J. Chem. 2021, 39, 1641–1645; Angew. Chem. Int. Ed. 2022, 61, e202208427)。在这些工作的基础上,王晓晨课题组设想发展一种硼/钯协同催化的体系,B(C6F5)3催化三烷基胺形成烯胺,钯催化剂与联烯反应生成烯丙基钯中间体;通过膦配体调节烯丙基钯的亲电性,促进烯胺进攻烯丙基钯,从而实现三烷基胺β位C-H键烯丙基化反应(如图1)。
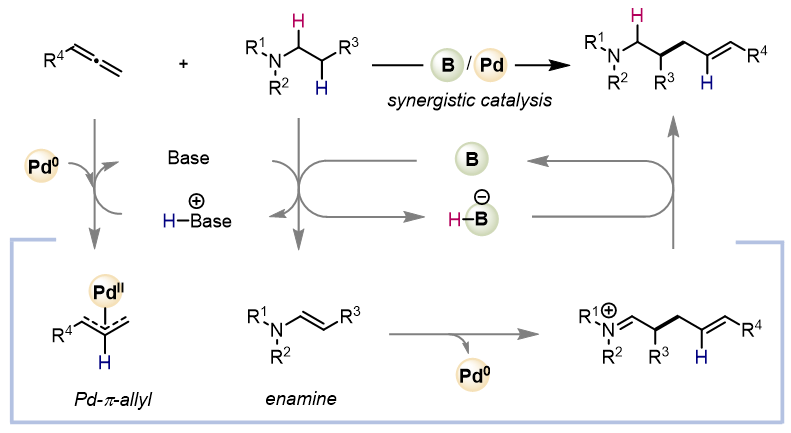
图1. 课题设计
基于此设想,作者使用N,N-二苄基-2-苯乙胺和1-苯基联烯作为模板底物进行了条件筛选,结果表明烯丙基化反应可以在B(C6F5)3与Pd催化剂协同催化下进行。其中,P(p-CF3C6H4)3配体对于反应活性至关重要,吸电子的三氟甲基通过诱导效应增强了烯丙基钯的亲电性。该反应具有良好的区域选择性以及底物范围,不仅能够兼容各种取代的三烷基胺以及芳基烷基取代的联烯,底物中含有酯基、醚键、炔基、烯基、卤素、酰胺等官能团也能够较好地反应。此外,该方法适用于天然产物和药物分子的后期官能团化修饰(如图2)。

图2. 底物拓展
随后,作者进行了克级实验、产物转化实验、机理实验,并提出了反应可能的机理(如图3)。在反应过程中,B(C6F5)3催化三烷基胺脱氢生成烯胺Ⅲ,Pd(0)被质子化形成Pd-H;Pd-H对联烯迁移插入,生成烯丙基钯中间体V;烯胺对烯丙基钯中间体进行亲核进攻,得到亚胺正离子IV;亚胺正离子被[B(C6F5)3-H]-还原,生成烯丙基化产物,同时再生催化剂。脱氢产生的负氢和质子分别由B(C6F5)3和钯催化剂转移到产物中,表现出优异的原子经济性。动力学实验表明,Pd(0)被质子化形成Pd-H的过程可能是反应的限速步。

图3. 可能的反应机理
综上所述,我校王晓晨课题组实现了首例三烷基胺β位C-H键烯丙基化反应。该方法不需要预先安装导向基团来控制区域选择性,体现了使用硼路易斯酸/过渡金属协同催化体系进行胺类化合物C-H键官能团化的优势,此外该工作也预示了其它金属有机亲电试剂在该策略中的潜在适用性,为后续研究奠定了基础。
这一成果近期发表在Angew. Chem. Int. Ed.上,文章的第一作者是我校博士研究生张鸣。
原文:
β-C–H Allylation of Trialkylamines with Allenes Promoted by Synergistic Borane/Palladium Catalysis
Ming Zhang, Zi-Lu Tang, Heng Luo, Xiao-Chen Wang
Angew. Chem. Int. Ed., 2023, DOI: 10.1002/anie.202317610
导师介绍
王晓晨
https://www.x-mol.com/university/faculty/63636




